Pressmeddelande -
EU godkänner Olumiant – ny tablettbehandling för vuxna med ledgångsreumatism
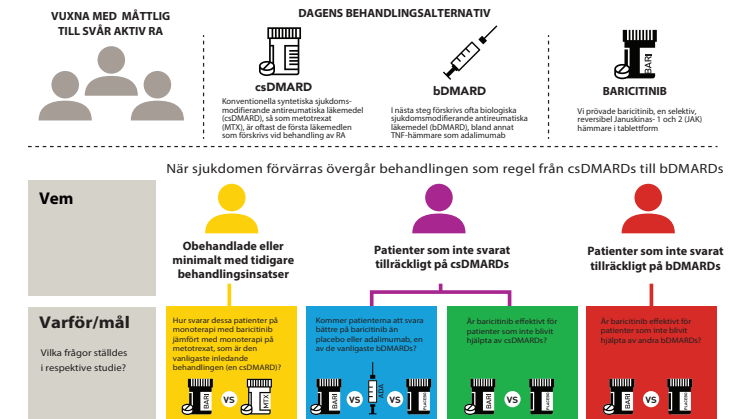
EU-kommissionen har godkänt Olumiant® (baricitinib) för behandling av måttlig till svår reumatoid artrit hos vuxna som inte svarar tillräckligt på konventionella sjukdomsmodifierande antireumatiska läkemedel eller när intolerans eller kontraindikation föreligger mot en eller flera av dessa behandlingar. Olumiant är en selektiv JAK1- och JAK2-hämmare i tablettform som tas en gång om dagen. Godkännandet innebär att patienter med ledgångsreumatism i Europa blir först med att få tillgång till detta helt nya behandlingsalternativ.
– Godkännandet är mycket glädjande och en viktig milstolpe för människor med måttlig till svår ledgångsreumatism säger Esbjörn Larsson, reumatolog och medicinsk rådgivare på Lilly. Trots kliniska framsteg finns det fortfarande patienter som dagligen brottas med smärta, extrem trött-het och ömmande, svullna leder. Vi är mycket hoppfulla att vi med nästa generations behandlingsmöjlighet i form av vår så kallad JAK-hämmare Olumiant, kan hjälpa dessa patienter snabbt må bättre.
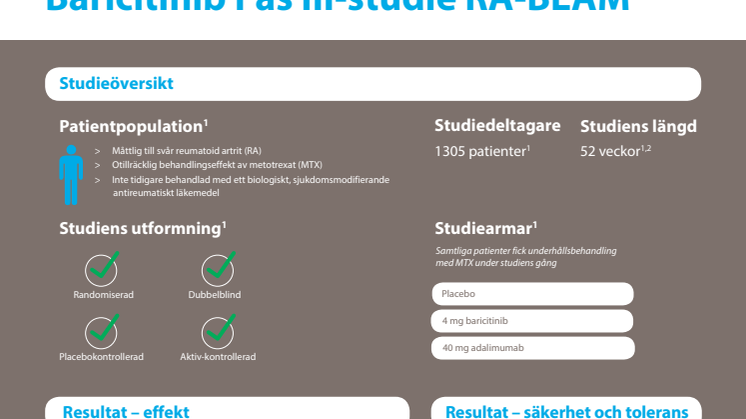
EU- godkännandet baseras på fem fas 3-studier (RA-BEGIN, RA-BEAM, RA-BUILD, RA-BEACON och RA-BEYOND) i vilka patienter med måttligt till svår aktiv reumatoid artrit behandlats med Olumiant. Studiedeltagarna representerade en bred patientpopulation däribland de som varit metotrexat-naiva samt de som haft otillräcklig effekt av behandling med metotrexat, konventionella sjukdomsmodifierande antireumatiska läkemedel (DMARDs) och TNF-hämmare.
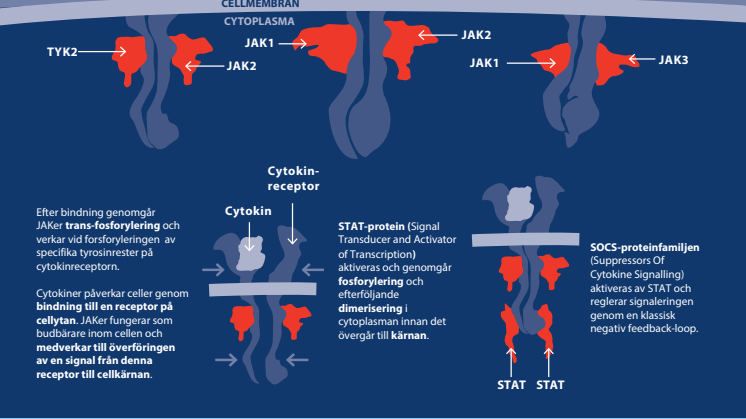
Olumiant (baricitinib) tillhör en ny klass av läkemedel, Januskinas (JAK)-hämmare, och är en ny tablettbehandling som ges en gång om dagen för behandling av måttlig till svår ledgångsreumatism. Cytokiner beroende av signalämnen, de s.k. JAK-enzymerna, har visat sig ha en roll i uppkomsten och utvecklingen av en rad inflammatoriska och autoimmuna sjukdomar, däribland ledgångsreumatism. Det finns i dag fyra kända JAK-enzymer: JAK1, JAK2, JAK3 och TYK2. Olumiant är en selektiv och reversibel hämmare av JAK1och JAK2 med mycket liten påverkan på JAK3.
Läs mer om EMAs beslut här
Mer information om det kliniska prövningsprogrammet för Olumiant finns på www.clinicaltrials.gov
För ytterligare information vänligen kontakta: Carin Landsmer, External Affairs Director, tel: 08-737 88 00
Ämnen
- Hälsa, sjukvård, läkemedel
Lilly är ett ledande globalt läkemedelsföretag som förenar vård och innovationer för att göra livet bättre för människor över hela världen. Lilly grundades för över ett hundra år sedan av en man som ville ta fram förstklassiga läkemedel som uppfyllde verkliga behov och detta är fortfarande den ambition som genomsyrar allt vi gör. Världen över arbetar Lillys medarbetare med att utveckla livsavgörande läkemedel för dem som behöver samt förbättra kunskapen om sjukdomar och möjlighet till behandling. Huvudkontoret ligger i Indianapolis, USA och det svenska kontoret i Solna.
SEBAR00045