Pressmeddelande -
Grönt ljus för Blincyto vid MRD-positiv leukemi
Den europeiska läkemedelsmyndighetens vetenskapliga kommitté för humanläkemedel, CHMP, rekommenderar EU-kommissionen att godkänna Blincyto för behandling av patienter med akut lymfatisk leukemi med kvarstående MRD (minimal kvarvarande sjukdom) vid komplett remission. Rekommendationen baseras på studiedata som visar att en behandlingscykel med Blincyto resulterade i att 78 procent av patienterna i studien inte längre hade detekterbar sjukdom.
– Det här är ett glädjande besked med tanke på att MRD-negativitet är den viktigaste prognostiska faktorn vid den här typen av leukemi, säger Per Bernell, hematolog och en av Sveriges ledande experter på ALL.
Akut lymfatisk leukemi, ALL, är en aggressiv form av blodcancer som varje år drabbar strax över hundra personer i Sverige. ALL utgår från omogna lymfocyter, en typ av vita blodkroppar, i benmärgen. Att leukemin räknas som akut innebär att sjukdomsförloppet kan vara hastigt och, om behandling inte sätts in, leda till döden inom loppet av ett par månader.
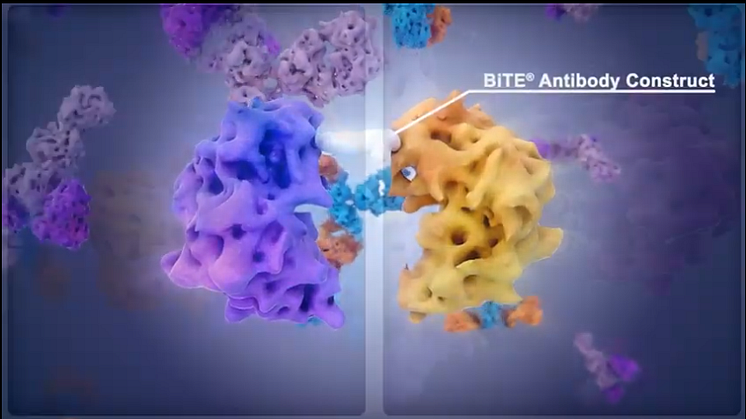
I november 2015 godkände EU-kommissionen Blincyto (blinatumomab), en så kallad BiTE-antikropp som stimulerar det egna immunsystemet att attackera leukemiceller, för behandling av vuxna med recidiverande eller refraktär Philadelphiakromosomnegativ CD19-positiv pre-B ALL. Tidigare i höst utvidgades indikationen till att även omfatta behandling av barn från ett års ålder.
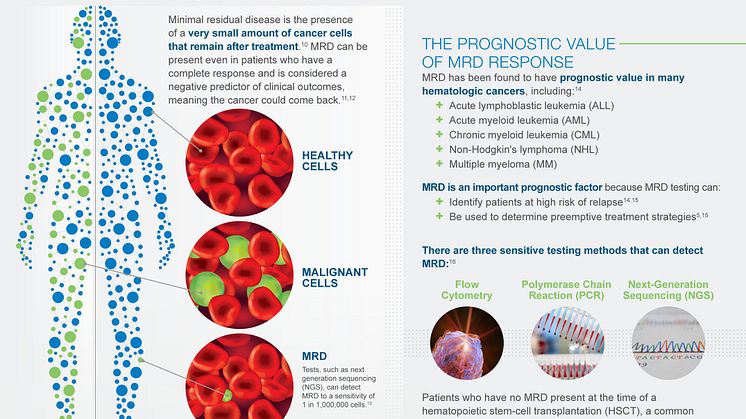
MRD (minimal residual disease), eller minimal kvarvarande sjukdom, betecknar den lilla mängd leukemiska celler som kan finnas kvar i benmärgen trots att patienten uppfyller kriterierna för komplett remission, alltså det läge där patienten inte längre uppvisar några symtom eller sjukdomstecken. Det råder idag konsensus om att MRD-negativitet är den starkaste prognostiska faktorn vid ALL.
– Hur väl man lyckas med att behandla bort de sista leukemicellerna spelar stor roll för prognosen, säger Per Bernell. Det blir tydligt när man tittar på femårsöverlevnaden som är hela 75 procent för MRD-negativa patienter medan motsvarande andel bland patienter med MRD endast uppgår till 33 procent.
I fas II-studien BLAST behandlades 116 ALL-patienter som uppnått komplett hematologisk remission efter minst tre intensiva behandlingar med cytostatika och hade MRD på en nivå av 10-3 eller högre. Efter en behandlingscykel med Blincyto hade 78 procent av patienterna uppnått komplett MRD-respons – ingen kvarvarande sjukdom kunde detekteras.
Baserat på dessa resultat har den europeiska läkemedelsmyndighetens vetenskapliga kommitté, Committee for Medicinal Products for Human Use, CHMP beslutat att rekommendera EU-kommissionen att godkänna ett utvidgande av marknadsföringstillståndet för Blincyto till att omfatta behandling av vuxna patienter med Philadelphiakromosomnegativ CD19-positiv pre-B ALL med MRD ≥10-3, vilket motsvarar 0,1 procent eller mer kvarvarande leukemiceller.
Kort om Blincyto
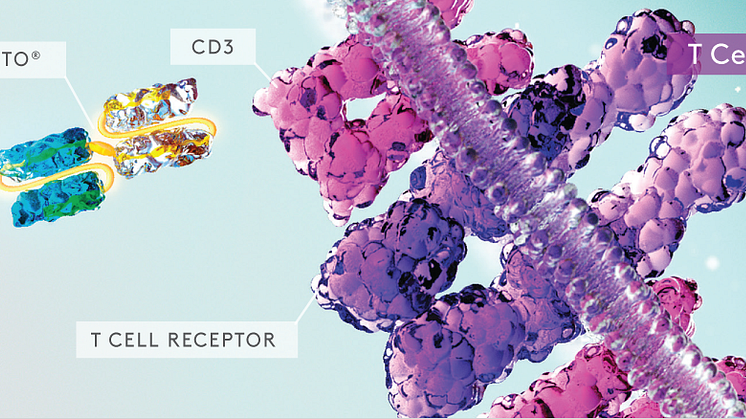
Blincyto (blinatumomab) bygger på Amgens immunterapeutiska plattform BiTE, Bi-specific T cell Engager. Blincyto är en bispecifik antikropp som binder dels till CD19, en ytmarkör på B-celler, dels till CD3 som finns på T-celler, en typ av celler som spelar en central roll i immunförsvaret. I de allra flesta fall uttrycker leukemicellerna hos patienter med B-ALL CD19. Blincyto kopplar således ihop leukemicellen med T-cellen och på så sätt stimuleras T-cellerna att attackera de CD19-positiva leukemicellerna. Blincyto har i kliniska studier visats öka andelen patienter som uppnår komplett remission/molekylär remission, vilket i sin tur är förknippat både med förlängd tid utan återfall och med förlängd total överlevnad. Vidare är det känt att patienter som genomgår stamcellstransplantation när de befinner sig i remission har påtagligt större chans att bli botade. Mer information om Blincyto (blinatumomab) finns på Fass.se.
Om BLAST
BLAST är den största prospektiva studien som genomförts på patienter med MRD-positiv ALL. Det är en öppen, multicenter-, enkelarms-, fas II-studie som utvärderar effekt, säkerhet och tolerabilitet av BLINCYTO hos vuxna patienter med MRD-positiv pre-B ALL vid komplett hematologisk remission efter tre eller flera cykler med intensiv kemoterapi. Patienterna i studien fick kontinuerlig IV-infusion med BLINCYTO 15 μg/m2/d under fyra veckor, följt av två veckor utan behandling. Patienterna fick upp till fyra behandlingscykler och kunde vid behov genomgå hematopoetisk stamcellstransplantation när som helst efter första cykeln. Det primära effektmåttet var andel som uppnådde icke detekterbar MRD inom en cykel av BLINCYTO-behandling och hematologisk återfallsfri överlevnad (RFS). De sekundära effektmåtten inkluderade incidens och svårighetsgrad av biverkningar, total överlevnad (OS), tid till hematologisk remission och varaktighet av komplett MRD-respons.
Säkerhet
Biverkningarna som beskrivs nedan har identifierats i kliniska studier på patienter med pre-B ALL (N = 843). De allvarligaste biverkningarna som kan uppstå vid behandling med blinatumomab inkluderar: infektioner (24,8%), neurologiska händelser (13,8%), neutropeni/febril neutropeni (10,1%), cytokinfrisättningssyndrom (3,3%) och tumörlyssyndrom (0,7%). De vanligast förekommande biverkningarna var: pyrexi (69,2%), infusionsrelaterade reaktioner (43,4%), infektioner med ospecificerad patogen (42,1%), huvudvärk (32,9%), anemi (22,8%), trombocytopeni (20,9%), febril neutropeni (20,2%), ödem (20,0%), neutropeni (19,7%), hudutslag (16,7%), förhöjda leverenzymer (16,1%), bakteriella infektioner (15,4%), tremor (15,2%), hosta (12,4%), leukopeni (13,4%), ryggsmärta (13,3%), frossa (13,0%), hypotension (12,8%), virusinfektioner (12,7%), minskad mängd immunglobuliner (12,5%), takykardi (11,3%), insomnia (10,7%), svampinfektion (10,6%) och smärta i extremiteter (10,2%). För ytterligare information om bland annat säkerhet, se internationellt pressmeddelande (på engelska).
För mer information, vänligen kontakta:
Maria Eriksson Svensson, medicinsk chef, Amgen, tel: 076–109 94 40
Relaterade länkar
Ämnen
Kategorier
Om Amgen
Alltsedan grundandet 1980 har Amgen varit en pionjär inom bioteknologi. Amgens strävan är att bekämpa allvarliga sjukdomar genom att ständigt expandera potentialen av biologiska läkemedel. Med utgångspunkt i en djupgående förståelse för humangenetiken och den mänskliga biologins grundläggande mekanismer söker Amgen identifiera nya viktiga signalvägar som kan ligga till grund för innovativa behandlingar för svårt sjuka individer.