Pressmeddelande -
Nya kliniska data på ESMO 2019 – respons i flera solida tumörtyper med KRAS G12C-hämmaren AMG 510
AMG 510, den första KRASG12C-hämmaren som nått klinisk fas, visar lovande resultat vid behandling av KRAS-muterad lung-, och kolorektalcancer. Det visar nya data som nu presenteras på ESMO 2019.
– Det är mycket hoppingivande att vi nu för första gången ser antitumöraktivitet hos patienter med kolorektalcancer med denna mutation, säger Bengt Glimelius, professor emeritus i onkologi vid Uppsala universitet och ledande expert på området.
Vid Europas största cancerkongress, European Society for Medical Oncology (ESMO), som just nu pågår i Barcelona presenteras nya data från en fas I-studie som utvärderar AMG 510, den första KRASG12C-hämmaren som nått klinisk fas,hos patienter med tidigare behandlade KRASG12C-muterade solida tumörer. Utöver lovande data vid lungcancer presenteras den första rapporterade evidensen någonsin för antitumöraktivitet hos patienter med KRASG12C-muterad kolorektalcancer och appendixcancer.
KRASG12C-mutationen förekommer hos cirka 13 procent av alla patienter med icke-småcellig lungcancer, 3–5 procent av kolorektalcancer och en till två procent av många andra solida tumörformer. Hittills har det, trots flera ambitiösa försök att angripa KRAS (KRASG12C är en av flera mutationer i KRAS-genen), inte funnits någon specifik behandling för KRASG12C-muterade tumörer eftersom det muterade proteinet har varit svårt eller rentav omöjligt att hämma med läkemedel.
Lovande resultat vid kolorektalcancer
Studien enrollerade 76 tungt förbehandlade patienter (median 4 behandlingslinjer) med KRASG12C-muterade solida tumörer. De data som nu presenteras vid ESMO avser de 55 patienter som var utvärderbara vid data-cutoff i juli 2019.
Av dessa 55 patienter hade 29 kolorektalcancer (CRC = colorectal cancer). Tolv fick måldosen 960 mg en gång dagligen och tio kvarstår på behandling. En patient i denna doskohort uppnådde partiell respons (PR = Partial Response) och tio uppnådde stabil sjukdom vilket ledde till en sjukdomskontroll (DCR = Disease Control Rate) på 92 procent.
– Prognosen för patienter med avancerad kolorektalcancer är fortsatt dålig såvida sjukdomen inte är relativt begränsad och kan opereras bort, säger Bengt Glimelius som sedan 1970-talet befunnit sig i tarmcancerforskningens frontlinje. Med tanke på att studien inkluderat enbart förbehandlade patienter som kan förväntas ha en median progressionsfri överlevnad på några månader är det uppmuntrande att det finns patienter som fortfarande står på behandling med måldosen efter mer än tre månader.
Data för 2 utvärderbara patienter med appendixcancer visade en partiell respons och en stabil sjukdom.
Fortsatt lovande vid svårbehandlad lungcancer
På ASCO tidigare i år presenterades data från de första försöken i människa med KRASG12C-hämmaren AMG 510 vid behandling av solida tumörer, däribland icke-småcellig lungcancer (NSCLC = non-small cell lung cancer). På ESMO presenteras nu en uppföljning av en större grupp patienter som inkluderar en undergrupp bestående av 34 NSCLC-patienter varav 23 kan utvärderas med avseende på effekt. Tretton av de utvärderbara patienterna fick måldosen 960 mg en gång dagligen, varav sju (54 procent) uppnådde partiell respons vid en eller flera tidpunkter och sex (46 procent) uppnådde stabil sjukdom och ingen hade progress vilket ledde till en sjukdomskontroll (DCR = Disease Control Rate) på 100 procent.
– KRAS-mutation är den vanligaste mutationen vid icke-småcellig lungcancer i Sverige och vi har tidigare inte haft någon specifik behandling att erbjuda. Patienterna har huvudsakligen fått generell cytostatikabehandling så detta är verkligen intressant. Det här är visserligen en liten studie i tidig fas, men de här resultaten är löftesrika och dessutom är det positivt att antitumöraktiviteten inte gett upphov till dosbegränsande toxicitet säger docent Jan Nyman, överläkare vid Sahlgrenska universitetssjukhuset i Göteborg och ordförande i Svenska Planeringsgruppen för lungcancer
– Dessa data indikerar också att det kan finnas relevanta molekylära skillnader mellan olika tumörtyper säger Sandra Eketorp Sylvan, senior medicinsk rådgivare på Amgen och specialst i onkologi. Med tanke på dessa resultat vid monoterapi och att vi inte sett någon dosbegränsande toxicitet initierar Amgen nu kombinationsstudier för AMG 510 inom NSCLC och kolorektalcancer. Inom kort startar även fas III-studier med AMG 510 som monoterapi vid NSCLC i Sverige.
Om AMG 510
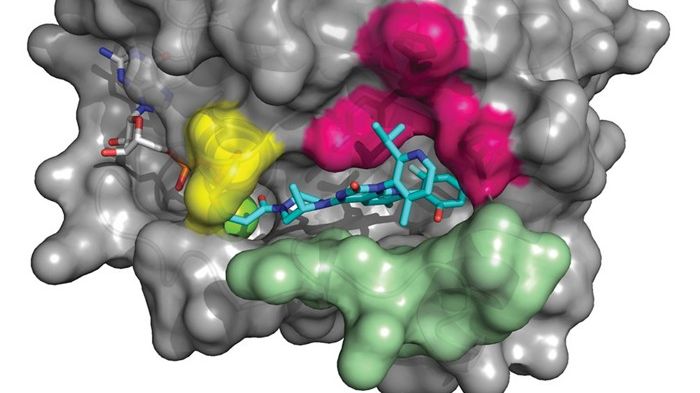
AMG 510 är en first-in-class small molecule som specifikt och irreversibelt binder till KRASG12C via den cysteinaminosyra som ersätter glycin när mutationen inträffar. KRASG12C blir på så vis låst i ett inaktivt GDP-bundet tillstånd (GDP = guanosine diphosphate, guanosindifosfat).
Den amerikanska läkemedelsmyndigheten FDA har givit AMG 510 orphan drug status avseende såväl NSCLC som metastaserad CRC (mCRC). FDA har även beviljat så kallad fast track designation för AMG 510 för behandling av patienter med tidigare behandlad metastaserande NSCLC med KRASG12C-mutation.
Om fas I-studien
Den nu aktuella fas I-studien är en öppen First in Human multicenterprövning som ingår i A Phase 1/2, Open-label Study Evaluating the Safety, Tolerability, Pharmacokinetics, Pharmacodynamics, and Efficacy of AMG 510 Monotherapy in Subjects With Advanced Solid Tumors With KRAS p.G12C Mutation and AMG 510 Combination Therapy in Subjects With Advanced NSCLC With KRAS p.G12C. I studien enrollerades patienter med KRASG12C-muterade solida tumörer som genomgått två eller fler tidigare behandlingar i enlighet med sin tumörtyp och sjukdomsfas.
Det primära effektmåttet i studien är säkerhet. Viktiga sekundära effektmått inkluderar farmakokinetik, objektiv svarsfrekvens (ORR = Objective Response Rate) bedömd var sjätte vecka, duration av respons (DOR = Duration of Response) och progressionsfri överlevnad. Patienterna delades in i fyra doskohorter, 180 mg, 360 mg, 720 mg och 960 mg, som administreras oralt en gång om dagen.
Vid utvärdering av tumörrespons definierades partiell respons (PR) i enlighet med RECIST 1.1 som en >30-procentig minskning av summan av diametern av mätbara lesioner (target lesions) jämfört med referensvärdet (före start av behandling).1 (RECIST = Response Evaluation Criteria in Solid Tumors)
Bland de 76 patienter som enrollerats i olika behandlingsgrupper står 52 kvar på behandling. Majoriteten av behandlingsrelaterade biverkningar var milda eller måttliga, grad 1 och 2. Endast två behandlingsrelaterade biverkningar var av grad 3, diarré och anemi. Inga biverkningar av grad 4 eller högre rapporterades.
Om KRAS
Mer än tre decennier av forskning har visat att RAS-genfamiljen är en av de mest muterade onkogenerna i human cancer (RAS = RAt Sarcoma virus).2,3 Inom denna familj är KRAS (Kirsten RAt Sarcoma virus) den vanligaste varianten och är särskilt ofta förekommande i solida tumörer.3 En specifik variant, KRASG12C, förekommer i cirka 13 procent av fallen av icke-småcellig lungcancer, 3–5 procent av kolorektal cancer och en till två procent av många andra solida tumörer.4 Amgen undersöker potentialen för KRASG12C-hämning för behandling av en mängd olika tumörtyper och är i färd med att initiera studier där AMG 510 kombineras med andra läkemedel vid behandling av lung- och kolorektalcancer.
- Eisenhauer EA, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1). Eur J Cancer. 2009;45:228–247.
- Cox A, et al. Drugging the undruggable RAS: Mission possible? Nat Rev Drug Discov. 2014 Nov;13(11):828–51.
- Fernandez-Medarde A, Santos E. RAS in cancer and developmental diseases. Genes Cancer. 2011 Mar;2(3):344–58.
- Lipford, JR. Pre-clinical development of AMG 510: the first inhibitor of KRASG12C in clinical testing. Oral presentation at AACR 2019; Atlanta, GA.March 29–April 3, 2019.
För ytterligare information, vänligen kontakta:
Maria Eriksson Svensson, medicinsk chef, Amgen, tel: 076–109 94 40
Ämnen
Kategorier
Om Amgen
Alltsedan grundandet 1980 har Amgen varit en pionjär inom bioteknologi. Amgens strävan är att bekämpa allvarliga sjukdomar genom att ständigt expandera potentialen av biologiska läkemedel. Med utgångspunkt i en djupgående förståelse för humangenetiken och den mänskliga biologins grundläggande mekanismer söker Amgen identifiera nya viktiga signalvägar som kan ligga till grund för innovativa behandlingar för svårt sjuka individer.