Pressmeddelande —
Forskare har hittat nyckeln till hur energi levereras in i cellernas ”transporthamn”
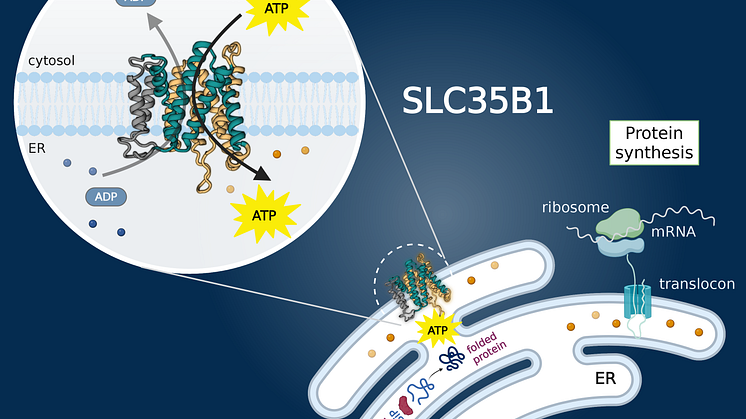
Forskare vid Stockholms universitet och SciLifeLab har hittat svaret på en av cellbiologins olösta gåtor, nämligen hur cellens energi, ATP, transporteras in det endoplasmatiska nätverket, ett nätverk av membran inuti cellen som proteiner och andra ämnen rör sig genom. Störning av energitransport kan påverka sjukdomar som typ 2-diabetes, cancer och neurodegenerativa sjukdomar. Studien är publicerad i Nature och identifierar transportproteinet SLC35B1 som porten.
Tillsammans med sin forskargrupp identifierade David Drew, professor i biokemi vid Stockholms universitet och SciLifeLab, proteinet SLC35B1 med hjälp av kryoelektronmikroskopi (cryo-EM), en metod som genom snabb nedfrysning möjliggör och förenklar avbildningen av biomolekyler. Resultatet är en första inblick i hur ATP tar sig in i det endoplasmatiska nätverket (ER), en livsviktig process som krävs för bland annat proteinveckning och hanteringen av kalcium.
– Trots decennier av forskning om funktionerna i det endoplasmatiska nätverket har frågan om hur ATP når insidan av ER varit oklar. Genom att bekräfta att proteinet SLC35B1 är transportören av ATP och se dess struktur genom kryoelektronmikroskopi har vi inte bara svarat på en grundläggande biologisk fråga, utan också öppnat nya vägar för framtida effektiva behandlingar, säger David Drew.
Framtida läkemedelsutveckling
De nya rönen har bred påverkan på hälsan. Störd aktivitet i ER är kopplad till sjukdomar som diabetes typ 2, cancer och neurodegenerativa sjukdomar, där stress i ER och problem med proteinveckning är bidragande orsaker. Med ny kunskap om SCL35B1 finns det nu möjlighet att utveckla bättre läkemedel.
– Att förstå hur energi levereras ger oss nya sätt att bemöta en rad sjukdomar som uppstår vid dysfunktionalitet i det endoplasmatiska nätverket. Att reglera aktiviteten i proteinet SLC35B1 skulle kunna bli en ny strategi för att återställa balansen i det endoplasmatiska nätverket vid sjukdomstillstånd, säger David Drew.
Hitta studien i Nature: ”Step-wise ATP translocation into the ER by human SLC35B1”
DOI: 10.1038/s41586-025-09069-w
Kontakt:
David Drew, Professor i biokemi vid Stockholms universitet och SciLifeLab
Kontakt: david.drew@dbb.su.se , 08-16 22 95
Läs mer om David Drews forskning:
Stockholm University https://www.su.se/english/prof...
SciLifeLab: https://www.scilifelab.se/rese...
Knut och Alice Wallenbergs stiftelse:
https://kaw.wallenberg.org/for...
https://kaw.wallenberg.org/for...
Relaterade länkar
Ämnen
Kategorier
Stockholms universitet bidrar till det hållbara demokratiska samhällets utveckling genom kunskap, upplysning och sanningssökande.
Prenumerera på universitetets nyhetsbrev om aktuell forskning, utbildning och samarbetsmöjligheter su.se/nyhetsbrev
Läs mer om universitetets forskning su.se/forskning
Bilderna i Mediearkivet är upphovsrättsligt skyddade. Bilderna får enbart användas i tydlig anslutning till nyheter kopplade till Stockholms universitet. Vid publicering anges alltid fotograf.